Le dernier Consensus de l’ACVIM sur la gestion de la maladie valvulaire du chien est sorti ! Cet article se propose de traduire et résumer l’article disponible librement publié en 2019 dans le JVIM suite à ce consensus :
Pathogénie de la Maladie Valvulaire Dégénérative du chien
En Amérique du Nord, 10% des chiens présentés en consultation auraient une affection cardiaque, la Maladie Valvulaire Degenerative (MVD) étant la pathologie la plus communes parmi les affections cardiaques, avec environ 75% des chiens cardiaques la présentant.
La MVD affecte davantage la valve mitrale, bien que la valve tricuspide soit impliquée elle aussi dans 30% des cas.
La maladie serait davantage représentée chez les mâles que chez les femelles (facteur 1,5), et chez les chiens de moins de 20 kg. La prévalence de la MVD augmente nettement avec l’âge chez les chiens de petite race, jusqu’à 85% montrant des signes de lésion valvulaire à 13 ans.
Bien que la cause de la MVD reste inconnue, la maladie semble avoir une composante héréditaire dans certaines races, et sa sévérité semble avoir une composante génétique dans d’autres races.
Une déformation progressive de la structure de la valve empêche à terme un ajustement des bords pour une fermeture efficace, permettant une régurgitation (fuite de la valve).
La régurgitation valvulaire progressive augmente le travail cardiaque, et conduit à un remodelage ventriculaire (hypertrophie excentrique de l’oreillette et du ventricule, …) et, finalement, à un dysfonctionnement ventriculaire.
La présence d’une lésion pathologique de MVD chez un individu n’identifie pas nécessairement un chien qui développera une régurgitation valvulaire importante ou des signes d’insuffisance cardiaque.

Il existe un classement de la MVD qui décrit 4 stades de base.

Stade A
Le stade A identifie les chiens à risque élevé de développer une maladie cardiaque mais qui ne présentent aucun trouble structurel identifiable du cœur (par exemple, un Cavalier King Charles Spaniel ou toute autre race prédisposée sans souffle cardiaque).
Stade B
Le stade B identifie les chiens atteints d’une maladie cardiaque structurelle, mais qui n’ont jamais développé de signes cliniques causés par une insuffisance cardiaque.
Contrairement aux recommandations de 2009, de solides données soutiennent désormais l’instauration d’un traitement visant à retarder l’apparition de signes cliniques d’insuffisance cardiaque chez un sous-groupe de patients au stade B2 présentant des modifications morphologiques cardiaques plus avancées.
Stade B1
Ainsi, le stade B1 décrit des chiens asymptomatiques qui ne présentent aucune preuve radiographique ou échocardiographique de remodelage cardiaque en réponse à leur MVD, ainsi que ceux chez lesquels des modifications de remodelage sont présentes, mais pas suffisamment sévères pour répondre aux critères des essais cliniques actuels qui ont été utilisés.
Stade B2
Le stade B2 concerne les chiens asymptomatiques présentant une régurgitation plus avancée de la valve mitrale, hémodynamiquement sévère et suffisamment ancienne pour avoir causé les constatations radiographiques et échocardiographiques d’hypertrophie de l’oreillette gauche et du ventricule répondant aux critères des essais cliniques permettant d’identifier les chiens bénéficiant d’un traitement pharmacologique afin de retarder l’insuffisance cardiaque.
Stade C
Le stade C désigne les chiens présentant des signes cliniques actuels ou passés d’insuffisance cardiaque causée par la MVD.
Stade D
Le stade D désigne les chiens atteints d’un MVD en phase terminale, dans lesquels les signes cliniques d’insuffisance cardiaque sont réfractaires au traitement standard. Ces patients ont besoin de stratégies de traitement avancées ou spécialisées pour rester cliniquement à l’aise avec leur maladie et, à un moment donné, les efforts de traitement deviennent vains sans réparation chirurgicale de la valve.

Propositions thérapeutiques
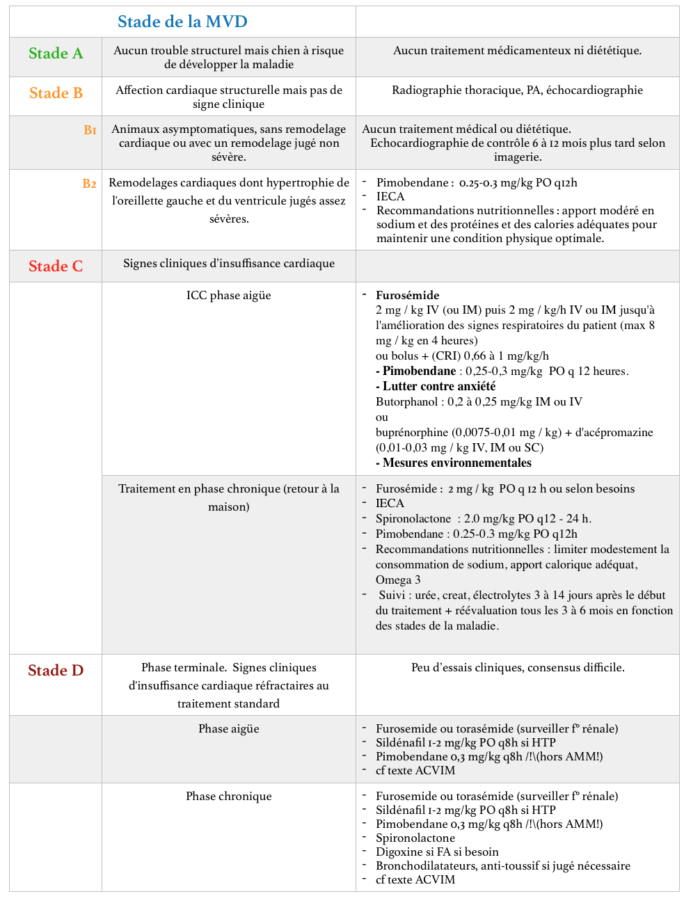
Pour les pressés, voici un tableau qui résume les propositions thérapeutiques de l’article en fonction des stades de MVD, issues du consensus. Je vous invite cependant à lire le texte complet car ce tableau ne cite pas les nuances apportées par les auteurs du consensus.
Stade A
Ce stade comprend les chiens présentant un risque d’insuffisance cardiaque plus élevé que la moyenne, mais sans anomalie structurelle apparente (c’est-à-dire sans souffle cardiaque audible) au moment de l’examen.
Les chiens de petite race, y compris ceux de race avec une prédisposition connue, comme par exemple les Cavalier King Charles Spaniels, les Teckels, … devraient faire l’objet d’évaluations régulières dans le cadre des soins de santé de routine.
Aucun traitement médicamenteux ni diététique n’est recommandé pour le moment.
Les animaux destinés à la reproduction doivent en être écartés si une indication échocardiographique de régurgitation mitrale est identifiée au cours de la tranche d’âge de reproduction normale (<6-8 ans).

Stade B
Les chiens appartenant au stade B présentent quant à eux une anomalie structurelle mais n’ont jamais présenté de signes cliniques associés.
Pour ces chiens, la MVD est souvent détectée lors d’un examen médical de routine, avec l’auscultation d’un souffle cardiaque typique de la régurgitation de la valve mitrale.
La radiographie thoracique est alors recommandée chez tous les patients, notamment pour disposer d’images « de base » à un moment où le patient est asymptomatique. En effet, cela pourrait nous aider plus tard à différencier les causes de toux d’origine cardiaque des causes non cardiaques.
De même, la mesure de la pression artérielle est recommandée, afin d’identifier ou exclure une hypertension systémique concomitante et pour établir la pression artérielle de base.
L’échocardiographie, est bien sûr nécessaire, afin d’identifier la cause du souffle entendu, et d’identifier des anomalies hémodynamiques, comme une hypertension pulmonaire ou une augmentation de la pression atriale gauche.
Bilan : examens complémentaires : radiographies thoraciques, pression artérielle, échocardiographie

Stade B1
Ce stade comprend les chiens asymptomatiques présentant une régurgitation de la valve mitrale causée par un MVD qui n’est pas suffisamment grave pour déclencher l’utilisation d’un traitement médical. Ainsi à ce stade, aucun traitement médical ou diététique n’est recommandé.
Les chiens de stade B1 peuvent présenter des dimensions de l’oreillette gauche et ventriculaire normales, avec une fonction systolique VG normale et un indice de Buchanan normal. Mais on retrouve aussi en stade B1 des animaux présentant une hypertrophie auriculaire et ventriculaire gauche.
Une échocardiographie de contrôle est alors proposée, 6 à 12 mois plus tard, en fonction des résultats de l’imagerie.
Stade B2
Il comprend les chiens avec une MVD asymptomatique provoquant une régurgitation mitrale suffisamment marquée pour entraîner un remodelage cardiaque (hypertrophie de l’ AG et du VG), suffisant pour recommander un traitement avant l’apparition des signes cliniques.
Les critères permettant de classer un animal en stade B2 sont les suivants :
- Intensité du souffle ≥ 3 / 6
- Rapport AG/Ao en coupe petit axe à droite en diastole précoce ≥1,6
- Diamètre interne du ventricule gauche en diastole, normalisé en fonction du poids corporel ≥ 1,7
- Indice de Buchanan (ajusté par race) > 10.5 ou un Indice de Buchanan « toutes races » ≥ 11,5 .. Valeur à moduler selon la race.
Idéalement, tous ces critères devraient être remplis avant de commencer le traitement, car ce dernier représente un engagement à vie.
Recommandations de traitement en stade B2
- Pimobendane : 0.25-0.3 mg/kg PO q12h
- IECA
- Recommandations nutritionnelles : apport modéré en sodium et des protéines et des calories adéquates pour maintenir une condition physique optimale.
Les beta bloquants ne sont pas recommandés en routine car les essais cliniques portant sur leur efficacité au stade B2 n’ont montré aucun bénéfice à ce jour. Quelques experts ont suggéré l’utilisation de bêta-bloquants, ou d’amlodipine à ce stade, mais des investigations supplémentaires sont nécessaires pour évaluer leur efficacité et leur sécurité dans ce cas, avant de pouvoir formuler des recommandations définitives.
De même, pour le moment, la spironolactone n’est pas indiquée à ce jour. En effet, les essais cliniques portant sur son efficacité en stade B2 n’ont pas été publiés à ce jour (2019), bien qu’une étude pilote suggèrerait que cette approche soit utilisée.
De plus, certains experts estiment que l’utilisation de médicaments contre la toux serait utile chez les patients occasionnels au stade avancé B2 lorsque l’on pense que leur toux résulte de la pression de l’hypertrophie cardiaque (sans œdème pulmonaire) sur les bronches adjacentes.
Enfin, une intervention chirurgicale consistant en une réparation de la valve mitrale est recommandée par certains experts, au stade avancé B2, pour les clients qui ont les moyens de se faire soigner dans les quelques centres présentant des preuves de taux de complications acceptables et de résultats efficaces et durables.

Stade C
Les chiens de stade C ont une MVD suffisamment grave pour provoquer des signes cliniques actuels ou passés d’insuffisance cardiaque.
En effet, ces patients continuent à être classés dans la phase C même après amélioration ou résolution complète de leurs signes cliniques avec un traitement standard. Dans des cas exceptionnels qui subissent une réparation chirurgicale de la valve mitrale chirurgicale, une reclassification au stade B est justifiée.
Pour les stades C et D, les soins aigüs de l’insuffisance cardiaque sont axés sur l’état hémodynamique du patient et l’apport tissulaire en oxygène
Les objectifs consistent à améliorer le débit cardiaque, à réduire les régurgitations de la valve mitrale et à atténuer les signes cliniques associés à un faible débit cardiaque ou à une augmentation excessive de la pression veineuse (congestion), en particulier un dysfonctionnement pulmonaire.
Les signes cliniques fréquents d’insuffisance cardiaque congestive (ICC) au stade C comprennent une tachypnée, une agitation, une détresse respiratoire ou de la toux.
Cependant, notons qu’il est important d’avoir en tête qu’une toux chez un chien présentant un souffle cardiaque apexien gauche, n’est pas toujours synonyme d’ICC. Ainsi, il est important d’effectuer des radiographies thoraciques (au moins 2 incidences) et idéalement un échocardiogramme, ainsi que des examens sanguins de routine (TP, créatinine, urée..).
Il est en effet important de réaliser une radiographie de face et de profil car chez certains chien on verra sur la vue de face une opacification du lobe caudal droit, sans opacification péri-hilaire. L’insuffisance rénale, en particulier, représente une comorbidité importante chez les chiens souffrant d’insuffisance cardiaque.
Le dosage des concentrations sériques de NT-proBNP peut être intéressant. En effet, une concentration de NT-proBNP normale chez un chien présentant des signes cliniques de toux, de dyspnée ou d’intolérance à l’exercice suggère fortement que l’insuffisance cardiaque n’est pas la cause des signes cliniques. On a cependant un chevauchement des valeurs entre les groupes lors de valeurs élevées de NT-pro BNP, et ces valeurs sont à prendre avec précautions. Ainsi, ce dosage est à envisager lors que l’on n’arrive pas à trancher et seules des valeurs basses permettent de nous orienter.
Traitements proposés en Stade C

Recommandations pour le traitement aigu (en milieu hospitalier) du stade C
Furosémide
à la dose de 2 mg / kg IV (ou IM), suivi de 2 mg / kg/h IV ou IM jusqu’à l’amélioration des signes respiratoires du patient (diminution de la fréquence et de l’effort respiratoires) (maximum de 8 mg / kg en 4 heures)
En cas d’œdème pulmonaire menaçant le pronostic vital (expectoration de mousse associée à une dyspnée sévère, radiographie du poumon blanc, réponse initiale médiocre au bolus de furosémide avec échec de l’effort respiratoire et amélioration du rythme sur 2 heures), le furosémide peut également être administré en perfusion à débit constant (CRI) à une dose de 0,66 à 1 mg/kg/heure après le bolus initial.
Pimobendane
à la dose de 0,25-0,3 mg / kg PO toutes les 12 heures.
Bien que les preuves cliniques soutenant l’utilisation chronique de pimobendane dans la prise en charge de l’insuffisance cardiaque de stade C par MVD soient plus solides que pour la présentation aiguë, la recommandation d’utiliser le pimobendane dans le traitement de l’insuffisance cardiaque aiguë serait fortement étayée par les preuves hémodynamiques et expérimentales. Dans de nombreux pays autres que les États-Unis, le pimobendane pour l’administration intraveineuse est disponible.
Prise en charge de l’anxiété
L’anxiété associée à la dyspnée doit être traitée, tout en surveillant la pression artérielle et la réponse respiratoire aux narcotiques et aux tranquillisants en cas d’insuffisance cardiaque aiguë.
Butorphanol : 0,2 à 0,25 mg / kg IM ou IV
ou
Association de buprénorphine (0,0075-0,01 mg / kg) et d’acépromazine (0,01-0,03 mg / kg IV, IM ou SC)
Mesures environnementales
Permettre au patient d’avoir librement accès à l’eau une fois que la diurèse a commencé.
Une supplémentation en oxygène, si nécessaire. Une thoracocenthèse peut être nécessaire lors de présence de liquide.
Maintenir la température et l’humidité de l’environnement, en augmentant le nombre d’oreillers sous la tête et en plaçant les patients sous sédation en sternal.
On remarquera que les IECA ne font pas partie des recommandations à ce stade en phase aigüe.
Recommandations pour le traitement chronique (à domicile) du stade C
- Furosémide : généralement à une dose de 2 mg / kg PO q 12 heures, ou selon les besoins pour préserver le confort du patient.
Certains experts choisissent maintenant de remplacer le furosémide par le torasémide à 1/10eme 1/ 20ème, soit environ 5% à 10% de la dose de furosémide, ou environ 0,1 à 0,3 mg / kg toutes les 24 heures. Cette molécule a montré une belle efficacité, mais des cas d’IRA ont été décrits… de plus amples études sont nécessaires sur cette molécule afin d’en établir la posologie et la fréquence d’administration ainsi que le rapport bénéfice/risque.
- IECA : 0,25- 0,5 mg / kg PO BID (par exemple, l’énalapril ou le benazepril)
- Spironolactone : 2.0 mg/kg PO q12 – 24 h. Principalement pour son effet antagoniste de l’aldostérone.
- Pimobendane : 0.25-0.3 mg/kg PO q12h
Une évaluation de la fonction rénale (urée, creat, électrolytes) est recommandée 3 à 14 jours après le début du traitement par le furosémide et/ou un IECA. On peut suspecter une faiblesse rénale et craindre une IRA si les concentrations sériques de créatinine augmentent d’au moins 30% par rapport à la concentration initiale.
Il est recommandé de réévaluer ces animaux tous les 3 à 6 mois en fonction des stades de la maladie.
Recommandations nutritionnelles
La cachexie serait un facteur pronostic négatif, et il est important de la prévenir, car elle est difficile à traiter. Ainsi, il est important de maintenir un apport calorique adéquat, par des mesures classiques comme tiédir la nourriture, mais cela implique aussi d’être vigilant à la survenue d’une anorexie et d’en trouver les causes. Il est ainsi intéressant de noter à chaque visite à la clinique la note d’état corporel et le poids.
Il est aussi recommandé de limiter modestement la consommation de sodium, en tenant compte de toutes les sources d’alimentation (aliments pour chiens, friandises, aliments de table et aliments utilisés pour administrer des médicaments) et d’éviter tout aliment transformé ou salé.
Il peut aussi être intéressant d’envisager une supplémentation en acides gras oméga-3, en particulier chez les chiens qui ont une perte d’appétit, une perte musculaire ou une arythmie.
Le propriétaire peut surveiller la fréquence respiratoire de l’animal notamment pendant son sommeil (et pas son repos). En effet, une FR< 25 mpm éloignerait l’hypothèse d’un ICC. (Ohad and al., Sleeping and resting respiratory rates in dogs with subclinical heart disease.J Am Vet Med Assoc. 2013 Sep 15;243(6):839-43.)
Stade D
Les patients présentent en stade D des signes cliniques d’échec, réfractaires au traitement standard de l’insuffisance cardiaque de stade C due à la MVD.
Peu d’essais cliniques ont porté sur l’efficacité et la sécurité des médicaments chez cette population de patients. En raison du manque relatif de données probantes issues des essais cliniques et des diverses présentations cliniques de patients atteints d’insuffisance cardiaque terminale, l’élaboration de directives pour ces patients s’est avérée difficile.
Ainsi, les chiens de stade D nécessitent une dose quotidienne de furosemide supérieure à 8 mg / kg ou une dose équivalente de torasémide, administrée en même temps que les doses standards des autres médicaments censés contrôler les signes cliniques d’insuffisance cardiaque (pimobendane, 0,3 mg / kg PO toutes les 12 heures, dose standard de IECA approuvé, et 2 mg / kg de spironolactone par jour).
Si nécessaire, des médicaments antiarythmiques pour maintenir le rythme sinusal ou réguler la réponse ventriculaire à la fibrillation auriculaire (fréquence cardiaque quotidienne moyenne <125 / minute) doivent être utilisés avant qu’un patient ne soit considéré comme réfractaire au traitement standard.
Une intervention chirurgicale pour réparer la valve mitrale au stade D est possible et indiquée dans la mesure du possible, bien qu’elle soit associée à une mortalité périopératoire plus élevée et à une survie globale réduite dans les études rapportées à ce jour.
Toutes les molécules abordées dans l’article source ne seront pas citées ici. Veuillez vous reposer à l’article du JVIM pour plus de précisions.
Traitements en stade D
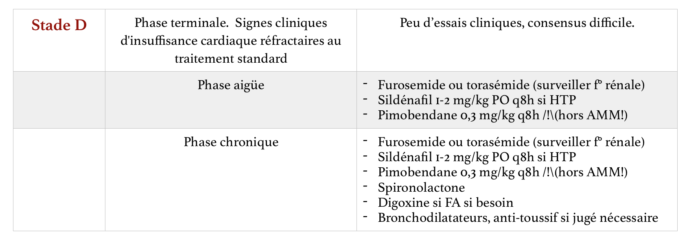
Recommandations pour le traitement aigu du stade D
En phase aigüe, on retrouve l’utilisation de furosemide ou torasemide (sauf en cas d’IRA).
Le sildénafil : 1 à 2 mg / kg PO q8 h et titrant si nécessaire peut être utilisé lors d’hypertension pulmonaire.
L’hypertension artérielle pulmonaire est reconnue comme une complication de plus en plus fréquente du MVD, soit comme conséquence directe d’une régurgitation sévère de la valve mitrale, soit comme une comorbidité indépendante pouvant être responsable de signes cliniques tels que syncope, toux et souffle court (dyspnée), et infiltrations pulmonaires parfois évidentes sur le plan radiographique.
La posologie de pimobendane peut être augmentée afin d’inclure une troisième dose quotidienne de 0,3 mg / kg de PO (c’est-à-dire 0,3 mg / kg de PO toutes les 8 heures); certains panélistes administrent une dose supplémentaire de pimobendane lors de l’admission chez des patients au stade D présentant un œdème pulmonaire aigu, quel que soit le moment de la dernière dose administrée à domicile. Cette posologie est hors AMM et doit être approuvée par le client.
Recommandations en phase chronique du stade D (retour à la maison) :
- La posologie de furosémide (ou du torasémide) peut être augmentée si nécessaire, si elle n’est pas limitée par un dysfonctionnement rénal (dont les indicateurs doivent généralement être surveillés 12 à 48 heures après l’augmentation de la posologie).
- La posologie de pimobendane peut être augmentée afin d’inclure une troisième dose quotidienne de 0,3 mg / kg de PO (c’est-à-dire 0,3 mg / kg de PO toutes les 8 heures) : utilisation hors AMM sous la responsabilité du praticien en informant le propriétaire.
- Le sildénafil : 1 à 2 mg / kg PO toutes les 8 heures
Il peut être utile dans la prise en charge des patients présentant des signes cliniques liés à l’effort et dans la prise en charge de l’ascite lorsqu’il existe des signes échocardiographiques d’hypertension artérielle pulmonaire modérée à sévère.
- La spironolactone, si elle n’a pas déjà été commencée comme recommandé au stade C, est indiquée pour le traitement chronique des patients au stade D.
Les bêta-bloquants ne doivent généralement pas être initiés à ce stade, sauf s’ils sont utilisés en complément du contrôle de la fréquence cardiaque en fibrillation atriale. Il convient de rester prudent en raison des effets inotropes négatifs des bêta-bloquants
Ainsi, la majorité des panélistes auraient estimé qu’il ne fallait pas arrêter les bêta-bloquants, mais que la réduction de la posologie pouvait être nécessaire si l’essoufflement ne pouvait pas être maîtrisé par l’ajout d’autres médicaments ou en présence de bradycardie, d’hypotension ou des deux.
La digoxine, utilisée aux mêmes doses (relativement faibles) recommandées par certains experts en insuffisance cardiaque de stade C avec fibrillation atriale, est recommandée pour le traitement de la fibrillation atriale chez les patients en stade D en absence de contre-indication.
Enfin, certains panelistes utilisent des anti-toussifs ou des bronchodilatateurs.

J’espère que cet article vous a aidé.
Retrouvez l’article complet source en libre accès, publié par les experts : ici
Auteur : Alexandra de Nazelle, Docteur vétérinaire, CEAV Médecine Interne
Praticienne et consultante
Date : Avril 2019
Bibliographie
Autres articles qui pourraient vous intéresser :
Lectures Médicales
- La cholangite féline
- Les obstructions urétérales félines: diagnostic et traitements
- Mise en place d’un bilan sénior chez les chiens âgés
- Le coup de chaleur : prise en charge
- Mise en place d’un bilan sénior chez les chiens âgés, un article basé sur le JVIM
- Pharmacocinétique de la gabapentine chez le chat : lecture d’un article

Management :
- Au delà des clivages générationnels
- Entre désirs et désillusions : les limitations économique des clients et leur impact sur votre pratique quotidienne et votre moral
- La méditation, pour les vétérinaires aussi ? et son article dans la presse vétérinaire
- Vétérinaire : le plus beau métier du monde ?

Rejoignez-moi sur les réseaux sociaux @Vet4Care
[instagram-feed]

